Chemia - zadanie.
sychu10 [ Pretorianin ]
Chemia - zadanie.
Zad.1
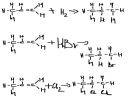
Posługując się wyłącznie wzorami strukturalnymi ułóż równania reakcji przyłączania wodoru, bromowodoru, chloru do cząsteczki propenu.
Zad.2
Ile gramów węgliku wapnia potrzeba do otrzymania 8 dm3 acetylenu ( warunki normalne )?
CaC2 + H2O -> C2H2 + Ca(OH)2
1 mol - 22,4 dm3
Proszę o pomoc.
Z góry dziękuję.
SULIK [ olewam zasady ]
Ad2.
1 mol gazu zajmuje objętość 22,4 dm3
x moli gazu zajmują objętość 8 dm3
x= 8*1/22,4 = 0,36 mola C2H2
CaC2 + 2H2O -> C2H2 + Ca(OH)2
z 1 mola CaC2 powstaje jeden mol C2H2
czyli analogicznie aby powstało 0,36 mola C2H2 należy użyć 0,36 mola CaC2
masa molowa CaC2 to 64,10 g/mol
1 mol CaC2 - 64,10 g
0,36 mola CaC2 - y
y = 0,36*64,10/1 = 23,08 g
więc musisz użyć 23,08 g CaC2 aby otrzymać 8 dm3 C2H2
Ad1.
rozrywasz podwójne wiązanie i przyłączasz go niego
a) H i H
b) H i Br
c) Cl i Cl
 --> Archiwum Forum
--> Archiwum Forum